Углекислый газ. Как соединяются неодинаковые атомы (молекулы углекислого газа) Графики сравнения потенциалов и сил
ОПРЕДЕЛЕНИЕ
Оксид углерода (IV) (углекислый газ) в обычных условиях представляет собой бесцветный газ, тяжелее воздуха, термически устойчивый, а при сжатии и охлаждении легко переходящий в жидкое и твердое («сухой лед») состояния.
Строение молекулы изображено на рис. 1. Плотность - 1,997 г/л. Плохо растворяется в воде, частично реагируя с ней. Проявляет кислотные свойства. Восстанавливается активными металлами, водородом и углеродом.
Рис. 1. Строение молекулы углекислого газа.
Брутто-формула углекислого газа - CO 2 . Как известно, молекулярная масса молекулы равна сумме относительных атомных масс атомов, входящих в состав молекулы (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел).
Mr(CO 2) = Ar(C) + 2×Ar(O);
Mr(CO 2) = 12 + 2×16 = 12 + 32 = 44.
ОПРЕДЕЛЕНИЕ
Молярная масса (М) - это масса 1 моль вещества.
Легко показать, что численные значения молярной массы М и относительной молекулярной массы M r равны, однако первая величина имеет размерность [M] = г/моль, а вторая безразмерна:
M = N A × m (1 молекулы) = N A × M r × 1 а.е.м. = (N A ×1 а.е.м.) × M r = × M r .
Это означает, что молярная масса углекислого газа равна 44 г/моль .
Молярную массу вещества в газообразном состоянии можно определить, используя понятие о его молярном объеме. Для этого находят объем, занимаемый при нормальных условиях определенной массой данного вещества, а затем вычисляют массу 22,4 л этого вещества при тех же условиях.
Для достижения данной цели (вычисление молярной массы) возможно использование уравнения состояния идеального газа (уравнение Менделеева-Клапейрона):
где p - давление газа (Па), V - объем газа (м 3), m - масса вещества (г), M - молярная масса вещества (г/моль), Т - абсолютная температура (К), R - универсальная газовая постоянная равная 8,314 Дж/(моль×К).
Примеры решения задач
ПРИМЕР 1
| Задание | Составьте формулу соединения меди с кислородом, если соотношение масс элементов в нём m(Cu) : m(O) = 4:1. |
| Решение | Найдем молярные массы меди и кислорода (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева округлим до целых чисел). Известно, что M = Mr, значит M(Сu) = 64 г/моль, а М(O) = 16 г/моль. n (Cu) = m (Cu) / M (Cu); n (Cu) = 4 / 64 = 0,0625 моль. n (О) = m (О) / M (О); n (О) = 1 / 16 = 0,0625 моль. Найдем мольное отношение: n(Cu) :n(O) = 0,0625: 0,0625 = 1:1, т.е. формула соединения меди с кислородом имеет вид CuO. Это оксид меди (II). |
| Ответ | CuO |
ПРИМЕР 2
| Задание | Составьте формулу соединения железа с серой, если соотношение масс элементов в нём m(Fe):m(S) = 7:4. |
| Решение | Для того, чтобы узнать, в каких отношениях находятся химические элементы в составе молекулы необходимо найти их количество вещества. Известно, что для нахождения количества вещества следует использовать формулу:
Найдем молярные массы железа и серы (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Известно, что M = Mr, значит M(S) = 32 г/моль, а М(Fe) = 56 г/моль. Тогда, количество вещества этих элементов равно: n (S) = m (S) / M (S); n (S) = 4 / 32 = 0,125 моль. n (Fe) = m (Fe) / M (Fe); n (Fe) = 7 / 56 = 0,125 моль. Найдем мольное отношение: n(Fe) :n(S) = 0,125: 0,125 = 1:1, т.е. формула соединения меди с кислородом имеет вид FeS. Это сульфид железа (II). |
| Ответ | FeS |
Диоксид углерода, оксид углерода, углекислота – все эти названия одного вещества, известного нам, как углекислый газ. Так какими же свойствами обладает этот газ, и каковы области его применения?
Углекислый газ и его физические свойства
Углекислый газ состоит из углерода и кислорода. Формула углекислого газа выглядит так – CO₂. В природе он образуется при сжигании или гниении органических веществ. В воздухе и минеральных источниках содержание газа также достаточно велико. кроме того люди и животные также выделяют диоксид углерода при выдыхании.

Рис. 1. Молекула углекислого газа.
Диоксид углерода является абсолютно бесцветным газом, его невозможно увидеть. Также он не имеет и запаха. Однако при его большой концентрации у человека может развиться гиперкапния, то есть удушье. Недостаток углекислого газа также может причинить проблемы со здоровьем. В результате недостатка это газа может развиться обратное состояние к удушью – гипокапния.
Если поместить углекислый газ в условия низкой температуры, то при -72 градусах он кристаллизуется и становится похож на снег. Поэтому углекислый газ в твердом состоянии называют «сухой снег».

Рис. 2. Сухой снег – углекислый газ.
Углекислый газ плотнее воздуха в 1,5 раза. Его плотность составляет 1,98 кг/м³ Химическая связь в молекуле углекислого газа ковалентная полярная. Полярной она является из-за того, что у кислорода больше значение электроотрицательности.
Важным понятием при изучении веществ является молекулярная и молярная масса. Молярная масса углекислого газа равна 44. Это число формируется из суммы относительных атомных масс атомов, входящих в состав молекулы. Значения относительных атомных масс берутся из таблицы Д.И. Менделеева и округляются до целых чисел. Соответственно, молярная масса CO₂ = 12+2*16.
Чтобы вычислить массовые доли элементов в углекислом газе необходимо следовать формулерасчета массовых долей каждого химического элемента в веществе.
n
– число атомов или молекул.
Ar
– относительная атомная масса химического элемента.
Mr
– относительная молекулярная масса вещества.
Рассчитаем относительную молекулярную массу углекислого газа.
Mr(CO₂) = 14 + 16 * 2 = 44 w(C) = 1 * 12 / 44 = 0,27 или 27 % Так как в формулу углекислого газа входит два атома кислорода, то n = 2 w(O) = 2 * 16 / 44 = 0,73 или 73 %
Ответ: w(C) = 0,27 или 27 %; w(O) = 0,73 или 73 %
Химические и биологические свойства углекислого газа
Углекислый газ обладает кислотными свойствами, так как является кислотным оксидом, и при растворении в воде образует угольную кислоту:
CO₂+H₂O=H₂CO₃
Вступает в реакцию со щелочами, в результате чего образуются карбонаты и гидрокарбонаты. Этот газ не подвержен горению. В нем горят только некоторые активные металлы, например, магний.
При нагревании углекислый газ распадается на угарный газ и кислород:
2CO₃=2CO+O₃.
Как и другие кислотные оксиды, данный газ легко вступает в реакцию с другими оксидами:
СaO+Co₃=CaCO₃.
Углекислый газ входит в состав всех органических веществ. Круговорот этого газа в природе осуществляется с помощью продуцентов, консументов и редуцентов. В процессе жизнедеятельности человек вырабатывает примерно 1 кг углекислого газа в сутки. При вдохе мы получаем кислород, однако в этот момент в альвеолах образуется углекислый газ. В этот момент происходит обмен: кислород попадает в кровь, а углекислый газ выходит наружу.
Получение углекислого газа происходит при производстве алкоголя. Также этот газ является побочным продуктом при получении азота, кислорода и аргона. Применение углекислого газа необходимо в пищевой промышленности, где углекислый газ выступает в качестве консерванта, а также углекислый газ в виде жидкости содержится в огнетушителях.

Рис. 3. Огнетушитель.
Что мы узнали?
Углекислый газ – вещество, которое в нормальных условиях не имеет цвета и запаха. помимо своего обычного названия – углекислый газ, его также называют оксидом углерода или диоксидом углерода.
Тест по теме
Оценка доклада
Средняя оценка: 4.3 . Всего получено оценок: 146.
Но если так отличаются молекулы из одних и тех же атомов, какое же разнообразие должно быть среди молекул из разных атомов! Давай-ка снова поищем в воздухе — может быть, мы найдём там и такие молекулы? Конечно, найдём!
Знаешь, какие молекулы ты выдыхаешь в воздух? (Разумеется, не только ты — все люди и все животные.) Молекулы твоего старого знакомого — углекислого газа! Пузырьки углекислого газа приятно пощипывают язык, когда ты пьёшь газированную воду или лисонад. Кусочки сухого льда, которые кладут в ящики с мороженым, тоже состоят из таких молекул; ведь сухой лёд — это твёрдая углекислота.
В молекуле углекислого газа два атома кислорода присоединились с разных сторон к одному атому углерода. «Углерод» — значит «тот, кто родит уголь». Но углерод рождает не только уголь. Когда ты рисуешь простым карандашом, на бумаге остаются маленькие чешуйки графита — они тоже состоят из атомов углерода. Из них же «сделаны» алмаз и обыкновенная сажа. Снова одни и те же атомы — и совершенно непохожие вещества!
Когда же атомы углерода соединяются не только между собой, но и с «чужими» атомами, тогда рождается столько разных веществ, что их и сосчитать трудно! Особенно много веществ рождается, когда атомы углерода соединяются с атомами самого лёгкого на свете газа — водородаю Все эти вещества называют общим именем — углеводороды, но у каждого углеводорода есть и своё собственное имя.
О простейшем из углеводородов говорится в известных тебе стихах: «А у нас в квартире газ — это раз!» Имя газа, который горит на кухне, — метан. В молекуле метана один атом углерода и четыре атома водорода. В пламени кухонной горелки молекулы метана разрушаются, атом углерода соединяется с двумя атомами кислорода, и получается уже знакомая тебе молекула углекислого газа. Атомы водорода тоже соединяются с атомами кислорода, и в результате получаются молекулы самого важного и нужного на свете вещества!
Молекулы этого вещества тоже есть в воздухе — их там полным-полно. Между прочим, в какой-то степени и ты к этому причастен, потому что выдыхаешь в воздух эти молекулы вместе с молекулами углекислого газа. Что же это за вещество? Если не догадался, подыши на холодное стекло, и вот оно перед тобой — вода!
Интересности:
Молекула вот такая малюсенькая, что если бы мы выстроили друг за другом сто миллионов молекул воды, то вся эта шеренга запросто поместилась между двух соседних линеек в твоей тетрадке. Но учёным всё-таки удалось узнать, как выглядит молекула воды. Вот её портрет. Правда, она похожа на голову медвежонка Винни-Пуха! Вон как ушки навострила! Конечно, никакие это не ушки, а два атома водорода, присоединившиеся к «голове» — атому кислорода. Но шутки шутками, а действительно — не имеют ли эти «ушки на макушке» какого-нибудь отношения к необыкновенным свойствам воды?
Градусов по Цельсию до конца века и если не увеличится приток углерода в почву. В соответствии с полученными данными исследователи делают вывод о том, что для компенсации выбросов углекислого газа из почвы необходимо в два–три раза увеличить количество лесной биомассы, а не на 70–80%, как утверждалось ранее. Исследование было проведено Финским институтом окружающей среды, Финским...
https://www.сайт/journal/123925
углекислого газа углекислого газа
https://www.сайт/journal/116900
Из Пенсильванского университета (США) в статье, опубликованной в журнале Nano Letters. Огромное количество углекислого газа , выбрасываемое в атмосферу промышленностью и транспортом, как полагают ученые, вызывает глобальное потепление. Обсуждается множество методов... и платины. Установка, собранная с использованием этого наноматериала позволила под воздействием солнечного света преобразовать смесь углекислого газа и паров воды в метан, этан и пропан в 20 раз эффективнее, чем при помощи...
https://www.сайт/journal/116932
Целью стимулировать фотосинтетическую активность водорослей и фитопланктона, или закачка сжиженного СО2 под землю. Конверсия углекислого газа в углеводороды с помощью наночастиц диоксида титана уже предлагалась учеными как еще один метод решения... меди и платины. Установка, собранная с использованием этого наноматериала позволила под воздействием солнечного света преобразовать смесь углекислого газа и паров воды в метан, этан и пропан в 20 раз эффективнее, чем при помощи обычных катализаторов...
https://www.сайт/journal/122591
США, слова которого приводит пресс-служба этого научного учреждения. Ученые обратили внимание на то, что поглощение растениями углекислого газа и испарение воды с поверхности их листьев происходит через одни и те же поры, называемые стоматами. Это... слишком большом содержании СО2 в воздухе стоматы листьев сужаются, вероятно, чтобы ограничить количество поступающего углекислого газа , используемого растениями для роста. Это приводит к замедлению испарения и снижению эффективности "природного...
https://www.сайт/journal/126120
Кристаллы были разработаны, используя простой метод, который опирается на три доступных химических вещества. Природный газ часто содержит углекислый газ и другие примеси, которые уменьшают эффективность этого топлива. Отрасли промышленности нуждаются в материале, который удалял бы углекислый газ . Идеальный материал должен быть доступным,избирательным и высокоемким и мог бы быть перезаряжен. Перезаряжающийся материал...
https://www.сайт/journal/126326
И сделали вывод, что, оказывается, мужчины ежегодно "выбрасывают" в атмосферу на две тонны углекислого газа больше, чем женщины. Исследователи объясняют это тем, что мужчины чаще пользуются автомобилем и, соответственно... половых различия, авторы исследования предлагают, таким образом, несколько иной способ в определении источников углекислого газа (один из газов ,влияющих на глобальное потепление) и, в частности, потребительские привычки и доходы, которые не учитываются в официальной...
https://www.сайт/journal/126887
В угленосных геологических формациях в штате Луизиана. Исследователи выяснили, что широко распространенные бактерии, использующие углекислый газ и сам уголь в качестве пищи, в присутствии воды могут дополнительно перерабатывать СО2 и выделять метан в... исследователей, для того, чтобы этот процесс работал, микроорганизмам, перерабатывающим СО2 в метан кроме самого углекислого газа и угля необходимы дополнительные питательные вещества - водород, соли уксусной кислоты и, что самое важное, ...
 Прапорщики и другие воинские звания: как они появились на самом деле Младший прапорщик в ссср
Прапорщики и другие воинские звания: как они появились на самом деле Младший прапорщик в ссср Можгинское медицинское училище министерства здравоохранения удмуртской республики Можгинское медицинское училище поступление
Можгинское медицинское училище министерства здравоохранения удмуртской республики Можгинское медицинское училище поступление Правильные многоугольники презентация к уроку по геометрии (9 класс) на тему Все о правильный многоугольник презентация
Правильные многоугольники презентация к уроку по геометрии (9 класс) на тему Все о правильный многоугольник презентация Таблица персонажи эпохи дворцовых переворотов
Таблица персонажи эпохи дворцовых переворотов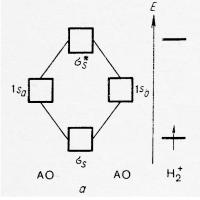 Метод молекулярных орбиталей (ММО)
Метод молекулярных орбиталей (ММО) Герундий - примеры использования - учим испанский язык
Герундий - примеры использования - учим испанский язык Методика определения ионов кальция и магния в природных водах
Методика определения ионов кальция и магния в природных водах