Гомогенным называется катализ при котором. Сущность и виды катализа
Скорость химических реакций может существенно возрасти под действием веществ, которые называют катализаторами .
Явление изменения скорости реакции при наличии катализаторов называют катализом, а реакции с их участием – каталитическими.
Катализатор – это простое или сложное вещество, которое принимает участие в химической реакции и изменяет ее скорость, но в конце остается в химически неизменном состоянии. Если скорость химической реакции под действием катализатора возрастает, то такой катализ называют позитивным, а если уменьшается – то негативным.
Каталитические свойства проявляют переходные металлы и их соединения – оксиды, гидроксиды, сульфиды, амины, аминокислоты и др. Они способны не только значительно ускорять реакции, но и изменять их механизм. Например, при взаимодействии оксида углерода (П) и водорода, в зависимости от природы катализатора, образуются разные продукты – метан или метанол.
В процессе окисления метана кислородом воздуха при наличии разных катализаторов можно получить метанол, формальдегид или муравьиную кислоту.
Катализаторы широко используют в производстве аммиака, серной, азотной, уксусной кислот, каучука, в процессах крекинга нефти, синтеза некоторых лекарственных препаратов и тому подобное. Реакции полимеризации, гидрирования и дегидрирования, получение спиртов, альдегидов, карбоновых кислот с достаточной для технических потребностей скоростью происходят только при наличии катализаторов.
Вещества, которые замедляют скорость химических реакций, называют ингибиторами .
Ингибиторы также широко используют в технике. Их название связано с тем химическим или биохимическим процессом, который они замедляют. В частности, вещества, которые уменьшают скорость коррозии металла, называют ингибиторами коррозии , а вещества, которые тормозят любые процессы окисления разных субстратов молекулярным кислородом, - антиоксидантами.
Катализаторы оценивают по определенным критериям, среди которых к наиболее важным принадлежат: активность, специфичность, стойкость к старению и отравлениям.
Активность определяют по отношению скоростей каталитической и некаталитической реакций. Катализатор тем активнее, чем больше он снижает величину энергии активации реакции.
Специфичность (выборочность) заключается в способности катализатора увеличивать скорость только одной реакции.
На активность катализаторов значительно влияют примеси. Одни из них могут усиливать, а другие – замедлять действие катализаторов. Вещества, которые сами не имеют каталитических свойств, но усиливают действие катализаторов, называют промоторами, или активаторами.
Известно также негативное действие некоторых химических веществ на активность катализаторов, так называемых каталитических ядов. Эти соединения частично, или полностью снижают активность катализаторов.
Одним из важных видов каталитических процессов является ферментный катализ , который происходит под действием катализаторов белковой природы: так называемых ферментов, или энзимов.
Ферменты как биологические катализаторы
Все химические процессы в условиях физиологичной среды организма (гидролиз, протолиз, фосфорелирование, комплексообразование, окислительно-восстановительные реакции) могут происходить только при участии катализаторов, которые называют ферментами, или энзимами.
Ферменты – это вещества белковой природы, которые производятся клетками живых организмов и значительно увеличивают скорость биохимических процессов.
Сейчас известно более 1800 ферментов, из которых много выделено в чистом кристаллическом виде. Считают, что в клетке содержится около 10 тыс. молекул разных ферментов, которые ускоряют свыше 2 тыс. реакций. Четвертая часть изученных в настоящее время ферментов содержат ионы разных металлов и поэтому их называют металлоферментами.
И ферменты, и неорганические катализаторы подчиняются общим законам катализа и характеризуются рядом общих признаков, то есть они:
катализируют только те реакции, которые являются энергетически возможными;
не изменяют направления хода реакций;
уменьшают энергию активации реакций, тем самым ускоряя их;
не расходуются в процессе реакции.
Однако ферменты характеризуются и особенными признаками, которые дают возможность отличить их от обычных неорганических катализаторов. Эти отличия связаны с особенностями строения ферментов, которые являются сложными макромолекулами белковой природы.
Катализ – это процесс изменения скорости химической реакции при помощи катализаторов – , принимающих участие в химической реакции, но в состав конечных продуктов не входящих и в результате реакции не расходующихся.
Одни катализаторы ускоряют реакцию (положительный катализ ), другие – замедляют (отрицательный катализ ). Отрицательный катализ называют ингибированием , а катализаторы, понижающие скорость химической реакции – ингибиторами .
Различают гомогенный и гетерогенный катализ.
Гомогенный катализ.
При гомогенном (однородном) катализе реагирующие вещества и катализатор находятся в одинаковом и между ними отсутствует поверхность раздела. Пример гомогенного катализа – реакция окисления SO 2 и SO 3 в присутствии катализатора NO (реагирующие вещества и катализатор являются газами).
Гетерогенный катализ.
В случае гетерогенного (неоднородного) катализа реагирующие вещества и катализатор находятся в различных агрегатных состояниях и между ними существует поверхность (граница) раздела. Обычно катализатор – твердое вещество, а реагирующие вещества – жидкости или газы. Пример гетерогенного катализа – окисление NN 3 до NO в присутствии Pt (катализатор – твердое вещество).
Механизм действия катализаторов
Действие положительных катализаторов сводится к понижению энергии активации реакции Е а(исх) , действие ингибиторов – противоположное.
Так, для реакции 2 HI = H 2 + I 2 Е а(исх) =184 кДж/моль. Когда же эта реакция протекает в присутствии катализатора Au или Pt , то Е а(исх) =104 кДж/моль, соответственно.
Механизм действия катализатора при гомогенном катализе объясняется образованием промежуточных соединений между катализатором и одним из реагирующих веществ. Далее промежуточное соединение реагирует со вторым исходным веществом, в результате чего образуется продукт реакции и катализатор в первоначальном виде. Так как скорость обоих промежуточных процессов значительно больше скорости прямого процесса, то реакция с участием катализатора протекает значительно быстрее, чем без него.
Например, реакция:
SO 2 +1/2 O 2 = SO 3 протекает очень медленно, а если использовать катализатор NO
то реакции NO +1/2О 2 = NO 2 и NO 2 + SO 2 = SO 3 + NO протекают быстро.
Механизм действия катализатора при гетерогенном катализе иной. В этом случае реакция протекает вследствие адсорбции молекул реагирующих веществ поверхностью катализатора (поверхность катализатора неоднородна: на ней имеются так называемые активные центры , на которых и адсорбируются частицы реагирующих веществ.). Увеличение скорости химической реакции достигается, в основном, за счет понижения энергии активации адсорбированных молекул, а также, отчасти, за счет увеличения концентрации реагирующих веществ в местах, где произошла адсорбция.
Каталитические яды и промоторы.
Некоторые вещества снижают или полностью уничтожают активность катализатора, такие вещества называют каталитическими ядами . Например, небольшие примеси серы (0,1%) полностью прекращает каталитическое действие металлического катализатора (губчатого железа), использующегося при синтезе аммиака. Вещества, повышающие активность катализатора, называют промоторами. Например, каталитическая активность губчатого железа значительно возрастает при добавлении примерно 2% метаалюмината калия KAlO 2 .
Применение катализаторов
Действие катализатора избирательно и специфично. Это означает, что, применяя различные катализаторы, из одних и тех же веществ можно получить различные продукты. Это особенно характерно для реакций органических веществ. Например, в присутствии катализатора AlO 3 происходит дегидратация этилового спирта, в присутствии Cu – дегидрирование:
Биологические катализаторы, принимающие участие в сложных химических превращениях, протекающих в организме, называются ферментами.
Катализаторы широко используются в производстве серной кислоты, аммиака, каучука, пластмасс и др. веществ.
Катализ нашел широкое применение в химической промышленности, в частности, в технологии неорганических веществ. Катализ – возбуждение химических реакций или изменение их скорости под влиянием веществ - катализаторов, многократно вступающих в химическое взаимодействие с участниками реакции и восстанавливающихся после каждого цикла взаимодействия свой химический состав. Существуют вещества, уменьшающие скорость реакции, которые называются ингибиторами или отрицательными катализаторами. Катализаторы не изменяют состояния равновесия в системе, а лишь облегчают его достижение. Катализатор может одновременно ускорять как прямую, так и обратную реакции, но при этом константа равновесия остается постоянной. Иными словами, катализатор не может изменить равновесие термодинамически невыгодных обратимых реакций, у которых равновесие сдвинуто в сторону исходных веществ.
Сущность ускоряющего действия катализаторов состоит в понижении энергии активации Е а химической реакции за счет изменения реакционного пути в присутствии катализатора. Для реакции превращения А в В реакционный путь можно представить следующим образом:
А + К АК
ВК В + К
Как видно из рисунка 1, вторая стадия механизма является лимитирующей, поскольку имеет наибольшую энергию активации Е кат, однако существенно более низкую, чем для некаталитического процесса Е некат. Снижение энергии активации происходит за счет компенсации энергии разрыва связей реагирующих молекул энергией образования новых связей с катализатором. Количественной характеристикой снижения энергии активации, а значит и эффективности катализатора может служить величина степени компенсации энергии разрываемых связей Дi:
= (Дi – Е кат)/Дi (1)
Чем ниже энергия активации каталитического процесса, тем выше степень компенсации.
Одновременно со снижением энергии активации во многих случаях происходит снижение порядка реакции. Понижение порядка реакции объясняется тем, что в присутствии катализатора реакции идет через несколько элементарных стадий, порядок которых может быть меньше порядка некаталитических реакций.
Виды катализа
По фазовому состоянию реагентов и катализатора каталитические процессы разделяют на гомогенные и гетерогенные. При гомогенном катализе катализатор и реагирующие вещества находятся в одной фазе (газовой или жидкой), при гетерогенном – в разных. Нередко реагирующая система гетерогенного каталитического процесса складывается из трех фаз в различных сочетаниях, например, реагенты могут быть в газовой и жидкой фазах, а катализатор – в твердой.
В особую группу выделяют ферментативные (биологические) каталитические процессы, распространенные в природе и применяемые в промышленности для производства кормовых белков, органических кислот, спиртов, а также при обезвреживании сточных вод.
По типам реакций катализ делят на окислительно-восстановительный и кислотно-основной. В реакциях, протекающих по окислительно-восстановительному механизму, промежуточное взаимодействие с катализатором сопровождается гомолитическим разрывом двухэлектронных связей в реагирующих веществах и образованием связей с катализатором по месту неспаренных электронов последнего. Типичными катализаторами окислительно-восстановительного взаимодействия являются металлы или оксиды переменной валентности.
Кислотно-основные каталитические реакции протекают в результате промежуточного протолитического взаимодействия реагирующих веществ с катализатором или взаимодействия с участием неподеленной пары электронов (гетеролитический) катализ. Гетеролитический катализ протекает с таким разрывом ковалентной связи, при котором, в отличие от гомолитических реакций, электронная пара, осуществляющая связь, целиком или частично остается у одного из атомов или группы атомов. Каталитическая активность зависит от легкости передачи протона реагенту (кислотный катализ) или отрыва протона от реагента (основной катализ) в первом акте катализа. По кислотно-основному механизму протекают каталитические реакции гидролиза, гидратации и дегидратации, полимеризации, поликонденсации, алкилирования, изомеризации и др. Активными катализаторами являются соединения бора, фтора, кремния, алюминия, серы и других элементов, обладающих кислотными свойствами, или соединений элементов первой и второй групп периодической системы, обладающих основными свойствами. Гидратация этилена по кислотно-основному механизму с участием кислотного катализатора НА осуществляется следующим образом: на первой стадии катализаторор служит донором протона
СН 2 =СН 2 + НА СН 3 -СН 2 + + А -
вторая стадия – собственно гидратация
СН 3 -СН 2 + + НОН СН 3 СН 2 ОН + Н +
третья стадия – регенерация катализатора
Н + + А - НА.
Окислительно-восстановительные и кислотно-основные реакции можно рассматривать по радикальному механизму, согласно которому образующаяся при хемосорбции прочная связь молекула-решетка катализатора способствует диссоциации реагирующих молекул на радикалы. При гетерогенном катализе свободные радикала, мигрируя по поверхности катализатора, образуют нейтральные молекулы продукта, которые десорбируются.
Существует также фотокатализ, когда процесс инициируется под действием света.
Поскольку в неорганической химии наиболее распространен гетерогенный катализ на твердых катализаторах, то на нем остановимся подробнее. Процесс можно разделить на несколько стадий:
1) внешняя диффузия реагирующих веществ из ядра потока к поверхности катализатора, в промышленных аппаратах обычно преобладает турбулентная (конвективная) диффузия над молекуларной;
2) внутренняя диффузия в порах зерна катализатора, в зависимости от размеров пор катализатора и размеров молекул реагентов диффузия может происходить по молекулярному механизму или по механизму Кнудсена (при стесненном движении);
3) активированная (химическая) адсорбция одного или нескольких реагирующих веществ на поверхности катализатора с образованием поверхностного химического соединения;
4) перегруппировка атомов с образованием поверхностного комплекса продукт-катализатор;
5) десорбция продукта катализа и регенерация активного центра катализатора, для ряда катализаторов активной является не вся его поверхность, а отдельные участки – активные центры;
6) диффузия продукта в порах катализатора;
7) диффузия продукта от поверхности зерна катализатора в поток газа.
Общая скорость гетерогенного каталитического процесса определяется скоростями отдельных стадий и лимитируется наиболее медленной из них. Говоря о стадии, лимитирующей процесс, предполагают, что остальные стадии протекают настолько быстро, что в каждой из них практически достигается равновесие. Скорости отдельных стадий определяются параметрами технологического процесса. По механизму процесса в целом, включая собственно каталитическую реакцию и диффузионные стадии переноса вещества, различают процессы, проходящие в кинетической, внешнедиффузионной и внутридиффузионной областях. Скорость процесса в общем случае определяется выражением:
d/d = k c (2)
где c – движущая сила процесса, равная произведению действующих концентраций реагирующих веществ, для процесса, протекающего в газовой фазе движущая сила выражается в парциальных давлениях реагирующих веществ р; k – константа скорости.
В общем случае константа скорости зависит от многих факторов:
k = f (k 1 , k 2 , k поб, …..D и, D и / , D п, ….) (3)
где k 1 , k 2 , k поб - константы скоростей прямой, обратной и побочной реакции; D и, D и / , D п - коэффициенты диффузии исходных веществ и продукта, определяющие значение k во внешне- или внутридиффузионной областях процесса.
В кинетической области k не зависит от коэффициентов диффузии. Общее кинетическое уравнение скорости газового каталитического процесса с учетом влияния на скорость основных параметров технологического режима:
u = kvpP n 0 = k 0 e -Ea/RT vpP n 0 (4)
где v - расход газа, p - движущая сила процесса при Р0,1 МПа (1 ат), P - отношение рабочего давления к атмосферному нормальному, то есть безразмерная величина, 0 - коэффициент пересчета к нормальному давлению и температуре, n - порядок реакции.
Механизм химических стадий определяется природой реагирующих веществ и катализатора. Процесс может лимитироваться хемосорбцией одного из реагентов поверхностью катализатора или десорбцией продуктов реакции. Скорость реакции может контролироваться образованием заряженного активированного комплекса. В этих случаях заряжение поверхности катализатора под действием каких-либо факторов оказывает существенное влияние на протекание реакции. В кинетической области протекают главным образом процессы на малоактивных катализаторах мелкого зернения с крупными порами при турбулентном течении потока реагентов, а также при низких температурах, близких к температурам зажигания катализатора. Для реакций в жидкостях переход в кинетическую область может происходить и с повышением температуры вследствие понижения вязкости жидкости и, следовательно, ускорения диффузии. С повышением температуры уменьшается степень ассоциации, сольватации, гидратации молекул реагентов в растворах, что приводит к росту коэффициентов диффузии и соответственно переходу из диффузионной области в кинетическую. Для реакций, общий порядок которых выше единицы, характерен переход из диффузионной области в кинетическую при значительном понижении концентрации исходных реагентов. Переход процесса из кинетической области во внешнедиффузионную может происходить при снижении скорости потока, повышении концентрации повышении температуры.
Во внешнедиффузионной области протекают прежде всего процессы на высокоактивных катализаторах, обеспечивающих быструю реакцию и достаточный выход продукта за время контакта реагентов с катализаторами, измеряемое долями секунды. Очень быстрая реакция почти полностью протекает на внешней поверхности катализатора. В этом случае нецелесообразно применять пористые зерна с высокоразвитой внутренней поверхностью, а нужно стремиться развить наружную поверхность катализатора. Так, при окислении аммиака на платине последнюю применяют в виде тончайших сеток, содержащих тысячи переплетений платиновой проволоки. Наиболее эффективным средством ускорения процессов, протекающих в области внешней диффузии, является перемешивание реагентов, которое часто достигается увеличением линейной скорости реагентов. Сильная турбулизация потока приводит к переходу процесса из внешнедиффузионной области во внутридиффузионную (при крупнозернистых мелкопористых катализаторах) или же в кинетическую области.
где G - количество вещества, перенесенное за время в направлении х, перпендикулярном к поверхности зерна катализатора при концентрации с диффундирующего компонента в ядре потока реагентов, S - свободная внешняя поверхность катализатора, dc/dx -градиент концентрации.
Предложено большое число способов и уравнений для определения коэффициентов диффузии веществ в различных средах. Для бинарной смеси веществ А и В по Арнольду

где Т - температура, К; М А, М В - молярные массы веществ А и В, г/моль; v А, v В - молярные объемы веществ; Р - общее давление (0,1 М Па); С А+В - константа Сезерленда.
Константа Сезерленда равна:
С А+В = 1,47(Т А / +Т В /) 0,5 (7)
г де
Т А / , Т В / -
температуры кипения компонентов А и В,
К.
де
Т А / , Т В / -
температуры кипения компонентов А и В,
К.
Для газов А и В с близкими значениями молярных объемов можно принимать =1, а при значительной разности между ними 1.
Коэффициент диффузии в жидких средах D ж можно определить по формуле

где - вязкость растворителя, ПаС; М и v - молярная масса и молярный объем диффундирующего вещества; х а - параметр, учитывающий ассоциацию молекул в растворителе.
Во внутридиффузионной области , то есть когда общая скорость процесса лимитируется диффузией реагентов в порах зерна катализатора, существует несколько путей ускорения процесса. Можно уменьшить размеры зерен катализатора и соответственно путь молекул до середины зерна, это возможно если переходят одновременно от фильтрующего слоя к кипящему. Можно изготовить для неподвижного слоя крупнопористые катализаторы, не уменьшая размеров зерен во избежание роста гидравлического сопротивления, но при этом неизбежно уменьшится внутренняя поверхность и соответственно понизится интенсивность работы катализатора по сравнению с мелкозернистым крупнопористым. Можно применять кольцеобразную контактную массу с небольшой толщиной стенок. Наконец, бидисперсные или полидисперсные катализаторы, в которых крупные поры являются транспортными путями к высокоразвитой поверхности, создаваемой тонкими порами. Во всех случаях стремятся настолько уменьшить глубину проникновения реагентов в поры (и продуктов из пор), чтобы ликвидировать внутридиффузионное торможение и перейти в кинетическую область, когда скорость процесса определяется только скоростью собственно химических актов катализа, то есть адсорбции реагентов активными центрами, образования продуктов и его десорбции. Большая часть промышленных процессов, проходящих в фильтрующем слое, тормозится внутренней диффузией, например крупномасштабные каталитические процессы конверсии метана с водяным паром, конверсии оксида углерода, синтез аммиака и т. д.
Время , необходимое для диффузии компонента в поры катализатора на глубину l, можно определить по формуле Эйнштейна:
= l 2 /2D э (10)
Эффективный коэффициент диффузии в порах определяют приближенно в зависимости от соотношения размеров пор и длины свободного пробега молекул. В газовых средах при длине свободного пробега молекулы компонента , меньшей эквивалентного диаметра поры d=2r (2r), принимают, что в порах происходит нормальная молекулярная диффузия D э =D, которую вычисляют по формуле:

При стесненном режиме движения, когда 2r, определяют D э =D к по ориентировочной формуле Кнудсена:
( 12)
12)
где r - поперечный радиус поры.
( 13)
13)
Диффузия в порах катализатора в жидких средах весьма затруднена вследствие сильного повышения вязкости раствора в узких каналах (аномальная вязкость), поэтому для катализа в жидкостях часто применяют дисперсные катализаторы, то есть мелкие непористые частицы. Во многих каталитических процессах с изменением состава реакционной смеси и других параметров процесса может меняться механизм катализа, а также состав и активность катализатора, поэтому необходимо учитывать возможность изменения характера и скорости процесса даже при относительно небольшом изменении его параметров.
Катализаторы могут неограниченно повышать константу скорости реакции, однако, в отличие от температуры, катализаторы не влияют на скорость диффузии. Поэтому, во многих случаях при значительном повышении скорости реакции общая скорость остается низкой из-за медленного подвода компонентов в зону реакции.
Определение катализа. Виды катализа . Хемосорбция и образование промежуточного активированного комплекса. Энергия активации каталитической реакции. Катализ и равновесие. Применение катализа.
Катализ – явление возбуждения химических реакций специальными веществами – катализаторами. Катализатор многократно вступает в промежуточное химическое взаимодействие с веществами, участвующими в реакции и восстанавливает свой состав после каждого цикла промежуточных взаимодействий.
Гомогенный катализ – реагирующие вещества и катализатор образуют одну фазу.
Гетерогенный катализ – вещества и катализатор находятся в разных фазах.
Микрогетерогенный катализ занимает промежуточное место между гомогенным и гетерогенным катализами. Катализатор – большие полимерные молекулы. Для взаимодействующих на них небольших молекул они подобны гетерогенным частицам, но образуют с реагентами одну фазу. В эту группу входят ферментативные реакции, в которых катализатор (фермент) – крупные белковые молекулы сложного состава и строения. Поэтому его называют и ферментативным катализом.
Химическое превращение протекает через образование активного комплекса, обладающего избыточной энергией. Ее достаточно для перестройки новых веществ – продуктов реакции. Изменение энергии системы при химическом взаимодействии по реакционному пути(1).
А – активированный комплекс
К –промежуточное соединение с катализатором
Е 0 , Е к – энергии исходных веществ и продуктов
Е 1 , Е 2 – энергии активации превращения прямом и обратном направлениях
∆Н – изменение энергии в результате превращения (тепловой эффект).
Но не все молекулы обладают достаточной энергией для образования активного комплекса – только те, энергия которых превышает энергию активации Е 1 . Если необходимая энергия Е 1 велика, то реакция практически не протекает.
Катализатор открывает новый реакционный путь, благодаря тому, что вступает в химическое взаимодействие с образованием активированного комплекса с меньшей энергией, чем требуется для образования активированного комплекса без катализатора. Промежуточное соединение, в которое входит катализатор, превращается далее в продукты через другой активированный комплекс, но тоже с меньшей энергией. После второго этапа реакции катализатор восстанавливает свой химический состав и его компоненты не входят в состав продуктов. И хотя реакционный путь удлиняется, становится стадийным, уменьшение энергии активированного комплекса приводит к увеличению скорости реакции (2).
Источник неизвестен
Особый интерес к катализу проявился в период развития промышленной химии, так как возможность ускорять химические реакции в нужном направлении без расхода энергии и по существу без расхода самого вещества катализатора придали катализу большую практическую значимость. С помощью катализа решаются задачи, стоящие перед технологией связанного азота, более 80% нефти перерабатывается с использованием каталитических процессов, невозможно осуществление большинства процессов органического синтеза.
Катализаторы – вещества, которые, многократно вступая в промежуточное взаимодействие с участниками реакции, изменяют ее механизм и увеличивают скорость реакции; при этом они восстанавливают свой химический состав после каждого цикла промежуточных воздействий.
Влияние катализатора на механизм химической реакции можно пояснить на условном примере. Пусть протекает одностадийная реакция с энергией активации Е 0:
Ход реакции на энергетической диаграмме каталитической и некаталитической реакций изображен кривой 1. В присутствии катализатора механизм реакции изменяется, она протекает через несколько последовательных стадий (кривая 2). Например, первой стадией может быть образование промежуточного активированного комплекса Акт:
А + Кт → АКт
Затем активированный комплекс реагирует со вторым реагентом с образованием комплекса катализатора и продукта:
АКт + В → RКт
Последней стадией является разложение комплекса RКт с образованием продукта К и высвобождением катализатора для нового каталитического цикла:
RКт → R +Кт
Каждая из этих последовательных стадий характеризуется своими значениями энергии активации Е 1 , Е 2 , Е 3 , но, как правило, высота каждого из этих потенциальных барьеров ниже энергии активации Е 0 . Таким образом, в присутствии катализатора реакция протекает по более энергетически выгодному пути, что позволяет проводить процесс с большей скоростью.
Исходное(I) и конечное (II) энергетические состояния реакционной системы в присутствии катализатора и без него остаются одинаковыми; следовательно: катализатор не может изменить состояние химического равновесия, которое не зависит от пути реакции.
Роль катализатора состоит лишь в изменении скорости достижения состояния равновесия. Катализатор может увеличить скорость только тех процессов, которые разрешены термодинамически, но не может инициировать термодинамически невозможные реакции.
Некоторые химические реакции без катализатора практически неосуществимы из-за слишком большой энергии активации. Казалось бы, что для преодоления высокого энергетического барьера можно повысить кинетическую энергию молекул, то есть увеличить температуру. Но для многих обратимых экзотермических реакций повышение температуры приводит к смещению равновесия в обратную сторону и делает реакцию неразрешенной термодинамически. В таких случаях применение катализаторов не только оправданно, но и необходимо. Катализатор снижает энергию активации и позволяет тем самым проводить ее при существенно более низких температурах.
Молекулы реагента адсорбируются на поверхности катализатора. Адсорбция представляет собой явление, связанное с уменьшением количества газа при соприкосновении газа (адсорбата) с твердым телом (адсорбентом), и заключается в некотором уплотнении газа на поверхности твердого тела. Различают физическую адсорбцию и хемосорбцию в зависимости от того, какова природа сил, вызывающих это концентрирование молекул адсорбата у поверхности твердого тела. Если эти силы имеют такую же природу, как и молекулярное воздействие в газах, жидкостях и твердых телах, то говорят о физической адсорбции. При хемосорбции проявляются силы взаимодействия химической природы – молекулы адсорбата теряют свою индивидуальность, образуя поверхностные соединения с адсорбентом.
При протекании каталитических процессов основная роль принадлежит хемосорбции, или активированной адсорбции, результатом которой является образование активированного комплекса адсорбции – неустойчивого промежуточного соединения между реагентом и катализатором. Стадия активированной адсорбции определяет специфичность действия катализаторов в отношении различных реакций. Если химическая связь реагента с адсорбентом слишком сильная, разрушение образования комплекса, ведущее к образованию продуктов, затрудняется. Если же связь адсорбента и адсорбата слишком слабая, близкая по своей природе к физической адсорбции, то в молекуле адсорбата не происходит разрыхления связей, приводящего к снижению энергии активации каталитического процесса по сравнению с некаталитическим.
Общая химическая технология, Кутепов А.М., Москва, Высшая школа, 1990, стр.206-207, 214, 205
Химия - наука о веществах и их превращениях, а также способах их получения. Даже в обычной школьной программе рассматривается такой важный вопрос, как типы реакций. Классификация, с которой знакомят школьников на базовом уровне, учитывает изменение степени окисления, фазу протекания, механизм процесса и т. д. Кроме того, все химические процессы подразделяют на некаталитические и каталитические реакции. Примеры превращений, протекающих с участием катализатора, встречаются человеку в обычной жизни: брожение, гниение. Некаталитические превращения нам встречаются гораздо реже.
Что такое катализатор
Это химическое вещество, которое способно менять скорость взаимодействия, но само в ней не участвует. В том случае, когда с помощью катализатора происходит ускорение процесса, идет речь о положительном катализе. В том случае, если добавляемое в процесс вещество снижает его называют ингибитором.

Виды катализа
Гомогенный и гетерогенный катализ отличаются по фазе, в которой находятся исходные вещества. Если исходные компоненты, взятые для взаимодействий, включая и катализатор, находятся в одном агрегатном состоянии, протекает гомогенный катализ. В том случае, когда в реакции принимают участие разные по фазе вещества, идет гетерогенный катализ.

Селективность действия
Катализ представляет собой не просто средство повышения производительности аппаратуры, он положительно влияет на качество получаемых продуктов. Объяснить подобное явление можно тем, что благодаря избирательному (селективному) действию большинства катализаторов, ускоряется прямая реакция, снижаются побочные процессы. В конечном итоге получаемые продукты имеют большую чистоту, нет необходимости дополнительно очищать вещества. Селективность действия катализатора дает реальное снижение непроизводственных затрат сырья, неплохую экономическую выгоду.

Преимущества применения катализатора в производстве
Чем еще характеризуются каталитические реакции? Примеры, рассматриваемые в обычной средней школе, свидетельствуют о том, что использование катализатора позволяет проводить процесс при более низких температурах. Эксперименты подтверждают, что с его помощью можно рассчитывать на существенное снижение энергетических затрат. Это особенно важно в современных условиях, когда в мире наблюдается недостаток энергетических ресурсов.
Примеры каталитических производств
В какой промышленности используют каталитические реакции? Примеры таких производств: изготовление азотной и серной кислот, водорода, аммиака, полимеров, Широко применяют катализ в получении органических кислот, одноатомных и фенола, синтетических смол, красителей, лекарственных средств.

Что является катализатором
В качестве катализаторов могут выступать многие вещества, находящиеся в периодической системе химических элементов Дмитрия Ивановича Менделеева, а также их соединения. Среди самых распространенных ускорителей выделяют: никель, железо, платину, кобальт, алюмосиликаты, оксиды марганца.

Особенности катализаторов
Помимо избирательного действия, у катализаторов отличная механическая прочность, они способны противостоять каталитическим ядам, легко регенерируются (восстанавливаются).
По фазовому состоянию каталитические подразделяют на газофазные и жидкофазные.
Подробнее рассмотрим такие типы реакций. В растворах ускорителем химического превращения выступают катионы водорода Н+, гидроксид ионы основания ОН-, катионы металлов М+ и вещества, которые способствуют образованию свободных радикалов.

Суть катализа
Механизм катализа при взаимодействии кислот и оснований состоит в том, что происходит обмен между взаимодействующими веществами и катализатором положительными ионами (протонами). При этом происходят внутримолекулярные превращения. По данному типу идут реакции:
- дегидратации (отцепления воды);
- гидратации (присоединения молекул воды);
- этерификации (образования сложного эфира из спиртов и карбоновых кислот);
- поликонденсации (образования полимера с отщеплением воды).
Теория катализа объясняет не только сам процесс, но и возможные побочные превращения. В случае гетерогенного катализа ускоритель процесса образует самостоятельную фазу, каталитическими свойствами обладают некоторые центры на поверхности реагирующих веществ либо задействуется вся поверхность.
Существует и микрогетерогенный процесс, который предполагает нахождение катализатора в коллоидном состоянии. Данный вариант является переходным состоянием от гомогенного к гетерогенному виду катализа. Большая часть таких процессов протекает между газообразными веществами с применением твердых катализаторов. Они могут быть в форме гранул, таблеток, зерен.
Распространение катализа в природе
Ферментативный катализ достаточно широко распространён в природе. Именно с помощью биокатализаторов протекает синтез белковых молекул, осуществляется обмен веществ в живых организмах. Ни один биологический процесс, протекающий с участием живых организмов, не обходит стороной каталитические реакции. Примеры жизненно важных процессов: синтез из аминокислот белков, специфичных для организма; расщепление жиров, белков, углеводов.
Алгоритм катализа
Рассмотрим механизм катализа. Данный процесс, протекающий на пористых твердых ускорителях химического взаимодействия, включает в себя несколько элементарных стадий:
- диффузия взаимодействующих веществ к поверхности крупинок катализатора из ядра потока;
- диффузия реагентов в порах катализатора;
- хемосорбция (активированная адсорбция) на поверхности ускорителя химической реакции с появлением химических поверхностных веществ - активированных комплексов «катализатор-реагенты»;
- перегруппировка атомов с возникновением поверхностных комбинаций «катализатор-продукт»;
- диффузия в порах ускорителя реакции продукта;
- диффузия продукта от поверхности зерна ускорителя реакции в ядро потока.
Каталитические и некаталитические реакции настолько важны, что ученые на протяжении многих лет продолжают исследования в данной сфере.
При гомогенном катализе нет необходимости сооружать специальные конструкции. Ферментативный катализ при гетерогенном варианте предполагает использование разнообразной и специфичной аппаратуры. Для его протекания разработаны специальные контактные аппараты, подразделяемые по поверхности контакта (в трубках, на стенках, катализаторных сетках); с фильтрующим слоем; взвешенным слоем; с движущимся пылевидным катализатором.
Теплообмен в аппаратах реализуется разными способами:
- путем применения выносных (внешних) теплообменников;
- с помощью теплообменников, встроенных в контактный аппарат.
Анализируя формулы по химии, можно найти и такие реакции, в которых катализатором выступает один из конечных продуктов, который образуется в ходе химического взаимодействия исходных компонентов.
Подобные процессы принято называть автокаталитическими, само явление в химии именуется автокатализом.
Скорость многих взаимодействий связана с присутствием в реакционной смеси определенных веществ. Их формулы в химии чаще всего упускаются, заменяются словом «катализатор» либо его сокращенным вариантом. Их не включают в итоговое стереохимическое уравнение, так как они после завершения взаимодействия не меняются с количественной точки зрения. В некоторых случаях достаточно незначительных количеств веществ, чтобы существенно повлиять на скорость осуществляемого процесса. Вполне допустимы и такие ситуации, когда в качестве ускорителя химического взаимодействия выступает сам реакционный сосуд.
Суть влияния катализатора на изменение скорости химического процесса в том, что данное вещество включено в состав активного комплекса, а потому изменяет химического взаимодействия.
При распаде данного комплекса наблюдается регенерация катализатора. Суть в том, что он не будет расходоваться, останется в неизменном количестве после окончания взаимодействия. Именно по этой причине вполне достаточно незначительного количества активного вещества для осуществления реакции с субстратом (реагирующим веществом). В реальности незначительные количества катализаторов при проведении все-таки расходуются, так как возможны различные побочные процессы: его отравление, технологические потери, смена состояния поверхности твёрдого катализатора. Формулы по химии не предполагают учет катализатора.
Заключение
Реакции, в которых принимает участие активное вещество (катализатор), окружают человека, к тому же они протекают и в его организме. Гомогенные реакции встречаются гораздо реже, чем гетерогенные взаимодействия. В любом случае сначала происходит образование промежуточных комплексов, которые являются нестабильными, постепенно разрушаются и наблюдается регенерация (восстановление) ускорителя химического процесса. К примеру, при взаимодействии метафосфорной кислоты с персульфатом калия в качестве катализатора выступает йодоводородная кислота. При ее добавлении к реагирующим веществам образуется раствор желтого цвета. По мере приближения к окончанию процесса окраска постепенно исчезает. В качестве промежуточного продукта в данном случае выступает йод, а процесс происходит в две стадии. Но как только метафосфорная кислота будет синтезирована, катализатор возвращается в свое первоначальное состояние. Катализаторы незаменимы в промышленности, они помогают ускорять превращения, получать качественные продукты реакции. Невозможны без их участия и биохимические процессы в нашем организме.
 Прапорщики и другие воинские звания: как они появились на самом деле Младший прапорщик в ссср
Прапорщики и другие воинские звания: как они появились на самом деле Младший прапорщик в ссср Можгинское медицинское училище министерства здравоохранения удмуртской республики Можгинское медицинское училище поступление
Можгинское медицинское училище министерства здравоохранения удмуртской республики Можгинское медицинское училище поступление Правильные многоугольники презентация к уроку по геометрии (9 класс) на тему Все о правильный многоугольник презентация
Правильные многоугольники презентация к уроку по геометрии (9 класс) на тему Все о правильный многоугольник презентация Таблица персонажи эпохи дворцовых переворотов
Таблица персонажи эпохи дворцовых переворотов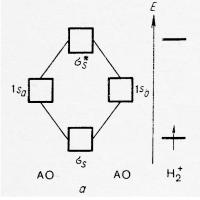 Метод молекулярных орбиталей (ММО)
Метод молекулярных орбиталей (ММО) Герундий - примеры использования - учим испанский язык
Герундий - примеры использования - учим испанский язык Методика определения ионов кальция и магния в природных водах
Методика определения ионов кальция и магния в природных водах