Диаграмма яблонского объяснение на примере пи связей. Флуоресцентные репортеры и их репортажи
Классификация электронных переходов
Диаграмма Яблонского
Физические процессы, протекающие в электронно-возбужденном состоянии молекул, принято представлять в виде диаграммы Яблонского. Основными безызлучательными процессами дезактивации нижнего возбужденного состояния S 1 являются внутренняя конверсия (переход между состояниями одинаковой мультиплетности) и интеркомбинационная конверсия (переход между состояниями разной мультиплетности, например, синглет-триплетный переход S 1 ®T 1 ). Внутренняя конверсия S 1 ®S 0 – сравнительно медленный процесс. Поэтому в возбужденном состоянии S 1 могут наблюдаться процессы спонтанного испускания фотона (спонтанное излучение) и фотохимические реакции. Излучательными процессами являются разрешенная по спину флуоресценция и запрещенная по спину фосфоресценция.
Электронные спектры поглощения в УФ и видимом диапазонах, дают важную информацию о структуре и свойствах электронно-возбужденных состояний молекул. Знание спектра поглощения вещества является обязательным условием фотолюминесцентных и фотохимических исследований. Кратко остановимся на классификации электронных переходов
Электроны в органической молекуле располагаются на молекулярных s-, p- и n -орбиталях. На каждой молекулярной орбитали помещаются два электрона, отличающихся спинами. При возбуждении молекулы светом происходит переход электрона с занятой связывающей орбитали на свободную разрыхляющую орбиталь. Такие переходы обозначают в соответствии с их орбитальной природой: s-s*, n -s*, p-p* и n -p*.
Полосы поглощения, обусловленные переходами s®s* , находятся преимущественно в вакуумной УФ области < 200 нм, где обычные спектрофотометры не применимы.
Переходам n -s* соответствуют полосы поглощения в УФ области. Например, органические соединения, содержащие n -электроны, локализованные на орбиталях гетероатомов, О, N, S, поглощают УФ свет в области около 200 нм.
Переходам p®p* и n ®p* соответствуют полосы поглощения в средней УФ-области. При сопряжении кратных связей полосы, обусловленные этими переходами, смещаются в ближнюю УФ- и видимую область спектра. Переходы n ®p* характерны для соединений, содержащих такие хромофорные группы, как С=О, C=S, N=N; эти переходы часто оказываются запрещенными, и соответствующие им полосы поглощения имеют сравнительно низкую интенсивность.
Эта классификация пригодна в основном для относительно простых молекул. В сложных молекулах определенный вклад в электронный переход могут вносить электроны, находящиеся на орбиталях разного типа.
Значительный интерес представляют электронные переходы с переносом заряда. Если в молекуле имеются электронодонорная и акцепторная группы, и они находятся в p-электронном сопряжении, то переход S 0 ®S 1 может сопровождаться переносом заряда от донора к акцептору по цепи сопряжения, как например, в данном стириловом красителе:
В этом случае говорят об электронном переходе с внутренним переносом заряда . Соответствующие полосы поглощения обычно характеризуются высокой интенсивностью и располагаются в видимой, а иногда и в ближней ИК области.
Для слабосвязанных органических донорно-акцепторных комплексов могут наблюдаться полосы поглощения, относящиеся к электронному переходу с переносом заряда от донора к акцептору через пространство (межмолекулярный перенос заряда ). Такие комплексы часто называют комплексами с переносом заряда. Длинноволновые полосы поглощения таких комплексов имеют сравнительно низкую интенсивность и могут находиться в ближней УФ, видимой и ближней ИК области спектра.
В металлорганической химии различают полосы поглощения, соответствующие переносу заряда от лиганда к металлу (ПЗЛМ ) и от металла к лиганду (ПЗМЛ ).
Федеральное
агентство морского
и речного транспорта
РФ
МОРСКОЙ
ГОСУДАРСТВЕННЫЙ
УНИВЕРСИТЕТ
имени
адмирала Г.И. Невельского
Морского физико-технического института
Курсовая работа по флуоресценции
Выполнил: Демиденко А. А.,
-
студент 20.31 группы
- Руководитель:
Майор А. Ю.
2010
Оглавление.
- Введение.
Глава 1 – основы спектроскопии.
- Диаграмма
Яблонского.
Характеристики испускания флуоресценции.
Стоксов сдвиг.
Независимость спектра испускания от длины волны возбуждения.
Правило зеркальной симметрии.
- Фото - электронный
умножитель.
Электронно - оптический преобразователь.
Приборы с зарядовой связью.
- Металл - окисел
- полупроводник (МОП-ёмкость).
Зарядовая связь.
Сдвиговый регистр с зарядовой связью.
Фоточувствительные приборы с зарядовой связью (ФПЗС).
- Проточный
лазерный флуориметр.
Малогабаритный ЛИФ спектрометр.
Список используемой литературы.
Введение
Решение
проблем окружающей среды и рационального
использования природных ресурсов
во многом зависит от разработки и
внедрения методов дистанционного
экспресс-анализа малых примесей
в атмосфере и воде. В естественных
водных средах такими примесями являются
биологическая связь, растворенные органические
и минеральные вещества, многочисленные
загрязнители. Большими возможностями
в анализе примесей располагает лазерная
спектроскопия, использующая комбинационное
рассеивание света, флуоресцентный анализ.
В
настоящее время для оперативного
мониторинга водных экосистем широко
применяют оптические методы позволяющие
определять концентрацию фитопланктона
и других веществ. Наибольшее распространение
получили спектральные методы. Особенно
актуальными такие исследования стали
после выявления прямой зависимости биологической
продуктивности морей и океана от содержания
в воде фитопланктона.
Определение
концентрации фитопланктона по оптическим
характеристикам морской среды может
выполняться пассивными и активными методами.
Первый широко используют с применением
авиа- и спутниковых носителей. Эти методы
основаны на измерении яркости отражаемой
от поверхности воды солнечной энергии
в широком диапазоне длин волн. Они позволяют
собирать масштабные данные о поверхности
водной среды, но имеют существенные ограничения:
малое пространственное разрешение и
невозможность измерения глубинных профилей.
Использование пассивных методов ограничивается
их не высокой точностью, что обусловлено
сильным влиянием состояния атмосферы
в месте проведения измерений.
Активные
методы основаны на облучении воды лазерным
лучом и регистрации спектра флуоресценции.
Различают лидарные, прокачиваемые и погружные
флуориметры. Самыми оптимальными
являются проточные флуориметры, которые
обладают высокой точностью и большим
пространственным разрешением.
Глава: 1
Основы
спектроскопии.
Люминесценция-
испускание фотонов из электронно-возбужденных
состояний – делится на два типа в зависимости
от природы основного и возбужденного
состояния. В синглетном возбужденном
состоянии электрон на энергетически
более высокой орбитали и второй электрон
на орбитали с более низкой энергией имеют
противоположную ориентацию спинов. Говорят,
что эти электроны спарены. В триплетном
состоянии эти электроны не спарены, т.е.
их спины имеют одинаковую ориентацию.
При возвращении электрона из возбужденного
сингнетного состояния в основное ориентация
его спина не должна меняться. Изменение
ориентации спина необходимо при переходе
из триплетного состояния в синглетное
основное состояние.
Флуоресценция-
это испускание, происходящее при
возвращении спаренного электрона
на более низкую орбиталь. Такие переходы
квантовомеханически “разрешимы”, а
типичные величины скоростей испускания
для них~10 8 с -1 . Высокие значения
скорости испускания приводят к временам
затухания флуоресценции 10 8 с(10 нс).
Время жизни- это средний период времени,
в течение которого флуорофор находится
в возбужденном состоянии. Фосфоресценция-
это испускание, происходящее при переходе
между состояниями различной мультиплетности,
как правило из возбужденного триплетного
состояния в синглетное основное. Такие
переходы не разрешены, и константы скорости
испускания малы. Типичный диапазон времени
затухания фосфоресценции - от миллисекунд
до секунд, что главным образом зависит
от вклада других процессов дезактивации.
Флуоресцентные
спектральные данные обычно представляют
в виде спектров испускания. Спектр испускания
флуоресценции - это зависимость интенсивности
флуоресценции от длин волн (в нанометрах)
или волновых чисел (в см -1). Два типичных
спектра испускания флуоресценции приведены.
Спектры испускания сильно изменяются
и зависят как от химической структуры
флуорофора, так и от растворителя, в котором
флуорофор рас творен. Спектры некоторых
соединений, таких, как перилен, имеют
четкую структуры, обусловленную отдельными
колебательными уровнями энергии основного
и возбужденного состояний. Другие состояния,
такие, как хинин, имеют спектры без колебательной
структуры.
1.1.
Диаграмма Яблонского
Поглощение и испускание света хорошо
иллюстрирует диаграмма уровней энергии,
предложенная Яблонским. Основное, первое
и второе электронные состояния обозначают
S 0 ; S 1 ; S 2
соответственно (рис. 1.а). Каждый из этих
уровней энергии может состоять из множества
колебательных энергетических уровней,
обозначаемых 0, 1, 2 и т. д. Переходы между
различными электронными уровнями обозначены
вертикальными линиями. Такое представление
используется, чтобы наглядно
РИС.1.а
Диаграмма Яблонского.
Рис. 1.б Диаграмма Яблонского.
Показать
мгновенную природу поглощения света.
Этот процесс происхо-дит примерно за
10 -18 с, время, слишком короткое для
заметного смещения ядер(принцип Франка-
Кондона).
Энергетическая
щель между различными колебательными
уровнями энергии видна из спектра испускания
перилена. Относительное число молекул
перилена, находящихся в колебательных
состояниях 0 и 1, описывается распределением
Больцмана.
1.2 Характеристики испускания
флуоресценции
Для
явления флуоресценции известно
несколько основных характеристик.
Существуют и исключения, но они редки.
Если какая-либо из нижеперечисленных
характеристик отсутствует у данного
флуорофора, можно сделать вывод о некоторых
особых свойствах этого соединения.
1.3.
Стоксов сдвиг
Рис.
2. Источником ультрафиолетового возбуждения
служил солнечный свет, пропущенный через
пластинку из голубого стекла. Перед приемником
в качестве желтого фильтра стоял стакан
с вином. Флуоресценция хинина лежит в
области 450 нм и поэтому хорошо заметна
невооруженным глазом. В настоящее время
для определения величины стоксова сдвига
используют другие методы.
Потери
энергии между возбуждением и испусканием
неизменно наблюдаются для флуоресцирующих
молекул в растворах. Одной из основных
причин возникновения стоксова сдвига
является быстрая релаксация на нижний
колебательный уровень состояния S 1 .
К тому же обычно происходит переход
РИС. 2. Схема первой установки для обнаружения стоксова сдвига.
на возбужденные колебательные уровни состояния S 0 (см. рис. 1), что приводит к дополнительной потере колебательной энергии. Вдобавок к этому стоксов сдвиг может быть еще более увеличен благодаря влияниям растворителя на флуорофоры к реакциям в возбужденных состояниях. В газовой фазе у атомов и молекул не всегда имеется стоксов сдвиг. Испускание без сдвига наблюдают тогда, когда концентрации газа достаточно малы для того, чтобы возбужденные молекулы не претерпевали столкновений с другими молекулами до процесса испускания. Такие столкновения приводят к релаксации. В жидкой фазе процессы соударения происходят непрерывно.
1.4. Независимость спектра испускания от длины волны возбуждения
Спектр испускания флуоресценции обычно не зависит от длины волны возбуждения. При возбуждении на высшие электронные и колебательные уровни избыток энергии быстро расходуется, переводя флуорофор на самый нижний колебательный уровень состояния S 1 . Эта релаксации происходит за время порядка 10 -12 с и является, по-видимому, результатом сильного перекрывания множества состояний с примерно равными энергиями. Благодаря такой быстрой релаксации длина волны возбуждения обычно не влияет на спектр испускания. Существуют исключения (например азулен), когда испускание может происходить как из S 2 , так и из S 1 - состояния. Кроме того, возбуждение на красном крае спектра поглощения часто ведет к сдвигу флуоресценции в длинноволновую область. Этот сдвиг обусловлен тем, что возбуждение на красном краю спектра избирательно возможно для тех флуорофоров, которые наиболее сильно взаимодействуют с растворителем.
1.5. Правило зеркальной симметрии
Обычно спектр испускания флуоресценции представляет собой зеркальное отражение спектра поглощения, точнее, того поглощения, которое соответствует переходу из S 0 в S 1 . Это особенно наглядно в случае перилена. Симметричная природа этих спектров определяется тем, что и поглощение, и испускание обусловлены одними и теми же переходами, а также сходством колебательных энергетических уровней состоянии S 0 и S 1 . Для многих молекул различное распределение электронов в состояниях S 0 и S 1 , существенно не влияет на эти уровни энергии. Согласно принципу Франка - Кондона, все электронные переходы происходят без изменения межъядерного расстояния. В результате, если данная вероятность перехода (фактор Франка - Кондона) между нулевым и вторым колебательными уровнями максимальна при поглощении, соответствующий переход будет наиболее вероятен также и в испускании (рис 3).
РИС. 3 Правило зеркальной симметрии и факторы Франка-Кондона
Глава: 2
Технические составляющие.
2.1-Фото
Электронный Умножитель
Фотоэлектронным
умножителем называют электровакуумный
прибор, преобразующей энергию оптического
излучения в электрические сигналы и содержащий
фотокатод, вторично-электронный умножитель
и анод. От вакуумного фотоэлемента ФЭУ
отличается тем, что кроме фотокатода
и анода содержит ещё фокусирующую
электронно-оптическую систему, диафрагму
и дополнительные электроды (диноды), являющиеся
эмиттерами вторичных электронов. (рис.
4)
При освещении
фотокатод 1 эмитирует первичные
фотоэлектроны, которые ускоряются
электрическим полем и фокусируются
электронно-оптической системой 2 на первый
динод Э 1 , вызывая его увеличенную
вторичную электронную эмиссию. Вторичные
электроны, вылетевшие из первого динода,
ускоряются электрическим полем и направляются
на второй динод Э 2 , увеличенный
поток электронов со второго динода направляется
на третий и т.д.
Электрическое
поле, ускоряющее электроны, создаётся
делителем постоянного напряжения,
обеспечивающим больший положительный
потенциал каждого последующего каскада
относительно предыдущего R1 – R11 .
Пространство
образуемое поверхностями фотокатода
1 и первого динода Э 1 с расположенными
между ними электродами, котодной (входной)
камерой ФЭУ Форма и распределение
электрического потенциала на поверхности
фотокатода фокусирующего электрода 2
и диафрагмы 3 должны обеспечить максимальный
сбор фотоэлектронов на первый динод за
счёт использования законов движения
электронов электрическом поле. Качество
электронно-оптической системы катодной
камеры определяется коэффициентом сбора
электронов Y k (отношением числа
фотоэлектронов, достигших первого динода,
к общему числу эмитированных фотокатодом
электронов n k) . Коэффициент сбора электронов у современных
ФЭУ близок к единице.
Первичные
фотоэлектроны, попадая на первый
динод, взаимодействуют с электронами
его вещества и возбуждают
их до более высоких энергетических
состояний. Часть электронов перемещается
к границе динода с вакуумом. Электроды,
которые достигают поверхности с энергией,
превышающей поверхностный потенциальный
барьер, переходя в вакуум и ускоряются
электрическим полем в направлении ко
второму диноду.
Рис.4 Устройство
ФЭУ со схемой его питания
2.2-Электронно Оптический Преобразователь
Рис
5
1-входное
окно
2-Защитная
плёнка
3-
Микроканальная пластина (МКП)
4-Фосфорный
экран
5-выходное
окно
Принцип действия
хорошо иллюстрирует рис. 5. Попадая в канал,
электрон испытывает соударения со стенкой
и выбивает вторичные электроны. В тянущем
электрическом поле этот процесс многократно
повторяется, позволяя получить коэффициент
усиления Nх10 4
и т.д.................
поглощение света. Закон Бугера Ламберта, бера
Поглощение света - это явление уменьшения интенсивности света при прохождении его через вещество. Уменьшение интенсивности света происходит в результате того, что энергия света переходит в другие виды энергии: энергию активизации, ионизации молекул, энергию теплового хаотического движения частиц в веществе и др. При прохождении монохроматического света через окрашенные растворы небольшой концентрации (С? 20%) и при условии, что растворитель не поглощает данную длину волны, интенсивность света также убывает по экспоненциальному закону. Закон поглощения света для окрашенных растворов называют законом Бугера-Ламберта-Бера: I= Io* e^- чcd, где С - концентрация раствора; ч - показатель поглощения для раствора единичной концентрации, зависит от природы растворенного вещества и длины волны падающего света.
Спектральные свойства и характеристики хромофоров. Диаграмма Яблонского
Хромофор - молекула, способная поглощать свет определенного диапазона длин волн.
Так, карбонильная группа СО является хромофором, поглощающим в области 280 нм, в то же время кетоны - бесцветные вещества.
Первичными стадиями фотобиофизического процесса являются поглощение света хромофорной группой и образование электронно- возбужденных состояний (ЭВС). При поглощении света молекулы, ионы, атомы, радикалы и другие типы частиц, участвующих в химических превращениях, могут переходить в электронно-возбужденные состояния. В них происходит изменение физических и химических свойств молекул по сравнению с основным состоянием. Меняются дипольный момент, геометрия, распределение электронной плотности, кислотно-основные свойства и т. д., и молекулы в возбужденном состоянии обладают иной реакционной способностью, что проявляется не столько в изменении скорости реакции, сколько в их ином, по сравнению с основным состоянием, направлении. Поглощение и испускание света хорошо иллюстрирует диаграмма уровней энергии, предложенная Яблонским
В основном состоянии все электроны занимают самые низшие электронные уровни и расположены на орбиталях попарно, причем их спины имеют противоположное направление (антипараллельны). Такое состояние молекулы называют синглетным невозбужденным (основным) состоянием и обозначают как S0. Так же обозначают энергетический уровень невозбужденной молекулы
При поглощении света происходит переход одного из электронов на вышележащую орбиталь, но его спин не меняется. Такое состояние молекулы и ее энергетический уровень обозначают как S1 или S2 в зависимости от того, на какой уровень перешел электрон. Это синглетное возбужденное состояние обозначают как S*. Основное, первое и второе электронные состояния обозначают S0, S1, и S2 соответственно. Каждый из этих уровней энергии может состоять из множества колебательных энергетических уровней, обозначаемых 0, 1, 2 и т. д. Влияние растворителя в данной схеме во внимание не принимается. Переходы между различными электронными уровнями обозначены вертикальными линиями. Такое представление используется, чтобы наглядно показать мгновенную природу поглощения света. Этот процесс происходит примерно за 10-15 с - время, слишком короткое для заметного смещения ядер.
Уровнями S 1 → S 0 {\displaystyle S_{1}\rightarrow S_{0}} или триплетными T 1 → T 0 {\displaystyle T_{1}\rightarrow T_{0}} . Типичное время жизни такого возбуждённого состояния составляет 10 −11 −10 −6 с.
Флуоресценцию следует отличать от фосфоресценции - запрещённого по спину излучательного перехода между двумя состояниями разной мультиплетности. Например, излучательный переход возбуждённого триплетного состояния T 1 в основное состояние S 0 . Синглет-триплетные переходы имеют квантовомеханический запрет, поэтому время жизни возбуждённого состояния при фосфоресценции составляет порядка 10 −3 −10 −2 с.
Происхождение термина [ | код ]
Термин «флуоресценция» происходит от названия минерала флюорит , у которого она впервые была обнаружена, и лат. -escent - суффикс, означающий слабое действие.
История изучения [ | код ]
Впервые флуоресценцию соединений хинина наблюдал физик Джордж Стокс в 1852 году.
Теоретические основы [ | код ]

Схематическое изображение процессов испускания и поглощения света. Диаграмма Яблонского [ | код ]
Схематически процессы поглощения света и флуоресценции показывают на диаграмме Яблонского.

При нормальных условиях большинство молекул находятся в основном электронном состоянии S 0 {\displaystyle S_{0}} . При поглощении света молекула переходит в возбуждённое состояние . При возбуждении на высшие электронные и колебательные уровни избыток энергии быстро расходуется, переводя флуорофор на самый нижний колебательный подуровень состояния S 1 {\displaystyle S_{1}} . Однако, существуют и исключения: например, флуоресценция азулена может происходить как из S 1 {\displaystyle S_{1}} , так и из S 2 {\displaystyle S_{2}} состояния.
Квантовый выход флуоресценции [ | код ]
Квантовый выход флуоресценции показывает, с какой эффективностью проходит данный процесс. Он определяется как отношение количества испускаемых и поглощаемых фотонов. Квантовый выход флуоресценции может быть рассчитан по формуле
Φ = N e m N a b s {\displaystyle \Phi ={\frac {N_{em}}{N_{abs}}}}где N e m {\displaystyle {N_{em}}} - количество испускаемых в результате флуоресценции фотонов, а N a b s {\displaystyle {N_{abs}}} - общее количество поглощаемых фотонов. Чем больше квантовый выход флуорофора , тем интенсивнее его флуоресценция. Квантовый выход можно также определить с помощью упрощённой диаграммы Яблонского , где Γ {\displaystyle {\Gamma }} и k n r {\displaystyle k_{nr}} - константы скорости излучательной и безызлучательной дезактивации возбуждённого состояния.
Тогда доля флуорофоров, возвращающихся в основное состояние с испусканием фотона, и, следовательно, квантовый выход:
Φ = Γ Γ + k n r {\displaystyle \Phi ={\frac {\Gamma }{\Gamma +k_{nr}}}}Из последней формулы следует, что Φ → 1 {\displaystyle \Phi \rightarrow 1} если k n r Γ → 0 {\displaystyle {\frac {k_{nr}}{\Gamma }}\rightarrow 0} , то есть если скорость безызлучательного перехода значительно меньше скорости излучательного перехода. Отметим, что квантовый выход всегда меньше единицы из-за стоксовых потерь.
Флуоресцентные соединения [ | код ]
Флюоресценция в ультрафиолетовом свете 0,0001 % водных растворов: голубым - хинина, зелёным - флуоресцеина, оранжевым - родамина-B, жёлтым - родамина-6G
К флуоресценции способны многие органические вещества, как правило содержащие систему сопряжённых π-связей. Наиболее известными являются хинин , метиловый зелёный, метиловый синий, феноловый красный, кристаллический фиолетовый, бриллиантовый синий кризоловый, POPOP, флуоресцеин , эозин , акридиновые красители (акридиновый оранжевый, акридиновый жёлтый), родамины (родамин 6G, родамин B) и многие другие.
Применение [ | код ]
В производстве красок и окраске текстиля [ | код ]
Флуоресцентные пигменты добавляются в краски , фломастеры , а также при окраске текстильных изделий, предметов обихода, украшений и т. п. для получения особо ярких («кричащих», «кислотных») цветов с повышенным спектральным альбедо в нужном диапазоне длин волн, иногда превышающим 100 %. Данный эффект достигается за счёт того, что флуоресцентные пигменты преобразуют содержащийся в естественном свете и в свете многих искусственных источников ультрафиолет (а также для жёлтых и красных пигментов, коротковолновую часть видимого спектра) в излучение нужного диапазона, делая цвет более интенсивным. Особой разновидностью флуоресцентных текстильных пигментов является оптическая синька , преобразующая ультрафиолет в излучение синего цвета, компенсирующее естественный желтоватый оттенок ткани , чем достигается эффект белоснежного цвета одежды и постельного белья . Оптическая синька применяется как при фабричной окраске тканей, так и для освежения цвета при стирке , в стиральных порошках . Аналогичные пигменты применяются и в производстве многих сортов бумаги, включая бумагу для повседневного офисного использования. В ней содержание пигмента с синькой, как правило, наибольшее.
В технике [ | код ]
В технические жидкости, например - антифризы , часто добавляют флюоресцентные добавки, облегчающие поиск течи из агрегата. В ультрафиолетовом свете подтёки такой жидкости становятся очень хорошо заметны.
В биологии и медицине [ | код ]
В биохимии и молекулярной биологии нашли применение флуоресцентные зонды и красители, которые используются для визуализации отдельных компонентов биологических систем. Например, эозинофилы (клетки крови) называются так потому, что имеют сродство к эозину , благодаря чему легко поддаются подсчёту при анализе крови .
Лазеры [ | код ]
Флуорофоры с высокими квантовыми выходами и хорошей фотостойкостью могут применяться в качестве компонентов активных сред лазеров на красителях.
В криминалистике [ | код ]
Отдельные флуоресцирующие вещества используются в оперативно-разыскной деятельности (для нанесения пометок на деньги, иные предметы в ходе документирования фактов дачи взяток и вымогательства. Также могут использоваться в химловушках)
Электронная спектроскопия
в супрамолекулярной химии
Основные разделы:
Физические основы поглощения света и фотолюминесценции
Техника измерения электронных спектров поглощения и люминесценции
Современные методы обработки спектроскопических данных
Примеры применения электронной спектроскопии для исследования свойств супрамолекулярных систем
Экспериментальные методы химии высоких энергий: Учебное пособие / Под общ. ред. М. Я. Мельникова. – М.: Изд-во МГУ, 2009. – 824 с
(ISBN 978-5-211-05561-2).
Е.Н. Ушаков / Самосборка и фотохимия супрамолекулярных систем на основе краунсодержащих непредельных соединений // дисс. док. хим. наук, ИПХФ РАН, Черноголовка, 2006. – 263 с.
Дополнительная литература:
E.N. Ushakov et al , Sandwich-type complexes of alkaline-earth metal cations with a bisstyryl dye containing two crown ether units, J. Phys. Chem. A, 1999, vol. 103, p. 11188-11193.
(имеется в электронном виде, PDF-файл, [email protected] )
I. Физические основы поглощения света и фотолюминесценции
Взаимодействие света с веществом
Свет, как известно, характеризуется длиной волны и частотой , которые связаны соотношением
где с – скорость света в вакууме, n – показатель преломления среды.
Волновую теорию света используют для интерпретации таких явлений как отражение, преломление, дифракция света, т.е. явлений, при которых свет не поглощается средой.
Однако для описания поглощения и испускания света веществом необходимо использовать квантовую теорию, согласно которой световая энергия может поглощаться только определенными порциями, или квантами. Энергия, переносимая одним квантом света, или, другими словами, фотоном, определяется уравнением Планка:

где h – постоянная Планка. То есть, монохроматический свет характеризуется не только длиной волны, но также и энергией фотона.
Поглощение монохроматического света гомогенной средой, содержащей поглощающее свет вещество, подчиняется закону ЛамбертаБера:

где I 0 – энергия монохроматического света, падающего за единицу времени на поверхность слоя вещества; I – энергия, прошедшая через слой вещества за единицу времени; l – толщина слоя, см; C – концентрация поглощающего свет вещества, моль/л; – молярный коэффициент поглощения (экстинкция), л/(мольсм), который зависит от природы вещества, длины волны света и температуры.
В фотохимии для характеристики поглощения обычно используют понятие оптическая плотность раствора (D , безразмерная величина)

Закон ЛамбертаБера не выполняется в тех случаях, когда значительная доля молекул переходит в возбужденное состояние (например, при очень высокой интенсивности падающего света). Отклонения от закона ЛамбертаБера иногда наблюдаются и при низких интенсивностях света. Однако эти отклонения являются кажущимися; как правило, они связаны либо с недостаточной разрешающей способностью спектрометра, либо с такими явлениями как ассоциация молекул.
Возбужденные электронные состояния
Используя слово свет, мы обычно подразумеваем оптическое излучение, видимое человеческим глазом. Спектральная кривая чувствительности человеческого глаза лежит в диапазоне 400 £ l £ 750 нм. Максимум чувствительности находится около 555 нм (зеленый свет). Для фотохимии интерес представляет более широкая область излучения, которую формально можно разделить следующим образом:
ближнее ультрафиолетовое (200 £ l £ 400 нм )
видимое (400 £ l £ 750 нм)
ближнее инфракрасное излучение (750 £ l £ 1000 нм)
При поглощении кванта света с l = 200–1000 нм возбуждаются внешние электроны молекулы, осуществляющие химическую связь; их возбуждение может приводить к химическому превращению. Этот спектральный диапазон является основным для спектроскопии поглощения и испускания света.
Спектры поглощения
Спектр поглощения вещества обычно состоит из полос разной интенсивности и ширины. Происхождение этих полос можно проиллюстрировать с помощью энергетической диаграммы молекулярных орбиталей (МО). Электроны в молекуле в основном состоянии располагаются парами на МО с разной энергией. Длинноволновая полоса в электронном спектре поглощения обычно соответствует переходу электрона с верхней занятой МО (ВЗМО) на нижнюю вакантную МО (НВМО). Полосы поглощения с большей энергией соответствуют переходам на вышележащие вакантные МО (например, S 0 S 2) или переходам с нижележащих занятых МО (например, S –1 S 1).
|
|
|
Структура и форма полосы поглощения
|
Полосы в спектрах поглощения нередко имеют определенную структуру. Это связано с тем, что каждому электронному состоянию соответствует набор разных колебательных состояний. На рисунке показана зависимость потенциальной энергии двухатомной молекулы в основном электронном состоянии от межъядерного расстояния (кривая S 0 ). Максимумы на кривых для колебательных состояний ( = 0, 1, 2, 3, 4) отвечают наиболее вероятным межъядерным расстояниям. Для нулевого колебательного состояния = 0 наиболее вероятное межъядерное расстояние находится в области минимума кривой потенциальной энергии. Для более высоких колебательных уровней наиболее вероятные межъядерные расстояния находятся вблизи точки поворота колебания. |
|
|
|
Принцип Франка Кондона Для объяснения относительной интенсивности переходов между колебательными уровнями основного и возбужденного электронных состояний используют принцип ФранкаКондона. Этот принцип основан на том, что электронный переход является намного более быстрым процессом (~10 15 с), чем движение ядер в молекуле (~10 13 с), то есть за время электронного перехода взаимное расположение ядер и их импульсы практически не изменяются. Поэтому электронно-колебательные переходы можно представить вертикальными линиями, соединяющими поверхности потенциальной энергии основного S 0 и возбужденного S 1 электронных состояний. Большинство молекул при комнатной температуре находится на нулевом колебательном уровне, поэтому фотоиндуцированные электронные переходы происходят именно с этого уровня. При данном расположении потенциальных кривых S 0 и S 1 наиболее вероятным электронно-колебательным переходом будет (0 2 )-переход. Интенсивность (0 0 )-перехода сравнительно мала, поскольку этому переходу соответствует маловероятное межъядерное расстояние. |
|
|
В многоатомной молекуле кривая потенциальной энергии переходит в многомерную поверхность, поэтому одному электронному переходу соответствует множество колебательных переходов. Часто эти колебательные переходы близки по энергии и им соответствует одна общая широкая полоса поглощения. Форма этой полосы, тем не менее, определяется принципом Франка-Кондона.
Процессы релаксации в электронно-возбужденных состояниях.
В жидких растворах при комнатной температуре электронно-возбужденные состояния молекул подвергаются сравнительно быстрым процессам релаксации электронно-колебательной энергии. Основные процессы релаксации: внутренняя конверсия из верхних возбужденных состояний S n в нижнее возбужденное состояние S 1 (< 10 12 с) и колебательная релаксация в состоянии S 1 , т.е. диссипация избыточной энергии колебаний в среде за счет столкновений возбужденных молекул вещества с молекулами среды (~10 11 с).

|
Эти процессы, как правило, происходят существенно быстрее по сравнению с процессом спонтанного испускания фотона, т.е. излучательной дезактивацией возбужденного состояния S 1 (~10 9 с). Поэтому излучательный переход из состояния S 1 в основное состояние S 0 , называемый флуоресценцией , происходит, как правило, из нулевого колебательного состояния. Таким образом, общим переходом при поглощении и испускании света является переход между нулевыми колебательными уровнями основного и возбужденного состояний, который называют (0 0 )-переходом. Энергия (0 0 )-перехода наименьшая при поглощении и наибольшая при испускании. Состояния S 0 и S 1 обычно имеют аналогичные распределения колебательных уровней по энергиям, поэтому спектр флуоресценции, как правило, близок к зеркальному отражению спектра поглощения, если оба спектра представлены в шкале энергии фотона. |
|
Стоксов сдвиг
Для сложных молекул в жидкой фазе (0 0 )-переход в спектре флуоресценции имеет меньшую энергию, чем (0 0 )-переход в спектре поглощения. Это связано с тем, что сразу после поглощения или испускания фотона молекула оказывается в неравновесном состоянии сольватации. В невязких растворителях при комнатной температуре переход возбужденного флуорофора в равновесное состояние сольватации происходит до испускания фотона. Поэтому (0 0 )-переход при испускании света имеет меньшую частоту, чем (0 0 )-переход при поглощении. Смещение полосы флуоресценции в красную область относительно длинноволновой полосы поглощения называется стоксовым сдвигом .

Мультиплетность
Мультиплетность электронного состояния равна n + 1, где n – число неспаренных электронов. Молекулярные орбитали молекул с четным числом электронов заполнены парами электронов с противоположно направленными спинами. Мультиплетность основного состояния большинства молекул с четным числом электронов равна 1, т.е. это синглетные состояния . При переходе электрона на верхнюю орбиталь его спин может оказаться ориентированным в том же или в противоположном направлении относительно оставшегося на нижней орбитали электрона. Если ориентации спина сохраняется, то мультиплетность возбужденного состояния, как и основного состояния, будет синглетным. Если же возбуждаемый электрон меняет направление спина, возбужденное состояние будет триплетным . Таким образом, одному основному состоянию соответствуют разные возбужденные состояния – синглетные и триплетные.

Диаграмма Яблонского
Физические процессы, протекающие в электронно-возбужденном состоянии молекул, принято представлять в виде диаграммы Яблонского. Основными безызлучательными процессами дезактивации нижнего возбужденного состояния S 1 являются внутренняя конверсия (переход между состояниями одинаковой мультиплетности) и интеркомбинационная конверсия (переход между состояниями разной мультиплетности, например, синглет-триплетный переход S 1 T 1 ). Внутренняя конверсия S 1 S 0 – сравнительно медленный процесс. Поэтому в возбужденном состоянии S 1 могут наблюдаться процессы спонтанного испускания фотона (спонтанное излучение) и фотохимические реакции. Излучательными процессами являются разрешенная по спину флуоресценция и запрещенная по спину фосфоресценция.

Классификация электронных переходов
Электронные спектры поглощения в УФ и видимом диапазонах, дают важную информацию о структуре и свойствах электронно-возбужденных состояний молекул. Знание спектра поглощения вещества является обязательным условием фотолюминесцентных и фотохимических исследований. Кратко остановимся на классификации электронных переходов
Электроны в органической молекуле располагаются на молекулярных -, - и n -орбиталях. На каждой молекулярной орбитали помещаются два электрона, отличающихся спинами. При возбуждении молекулы светом происходит переход электрона с занятой связывающей орбитали на свободную разрыхляющую орбиталь. Такие переходы обозначают в соответствии с их орбитальной природой: *, n *, * и n *.
Полосы поглощения, обусловленные переходами * , находятся преимущественно в вакуумной УФ области < 200 нм, где обычные спектрофотометры не применимы.
Переходам n * соответствуют полосы поглощения в УФ области. Например, органические соединения, содержащие n -электроны, локализованные на орбиталяхгетероатомов, О, N, S, поглощают УФ свет в области около 200 нм.
П ереходам * и n * соответствуют полосы поглощения в средней УФ-области. При сопряжении кратных связей полосы, обусловленные этими переходами, смещаются в ближнюю УФ- и видимую область спектра. Переходы n * характерны для соединений, содержащих такие хромофорные группы, как С=О, C=S, N=N; эти переходы часто оказываются запрещенными, и соответствующие им полосы поглощения имеют сравнительно низкую интенсивность.
Эта классификация пригодна в основном для относительно простых молекул. В сложных молекулах определенный вклад в электронный переход могут вносить электроны, находящиеся на орбиталях разного типа.
Значительный интерес представляют электронные переходы с переносом заряда. Если в молекуле имеются электронодонорная и акцепторная группы, и они находятся в -электронном сопряжении, то переход S 0 S 1 может сопровождаться переносом заряда от донора к акцептору по цепи сопряжения, как например, в данном стириловом красителе:

В этом случае говорят об электронном переходе с внутренним переносом заряда . Соответствующие полосы поглощения обычно характеризуются высокой интенсивностью и располагаются в видимой, а иногда и в ближней ИК области.
Для слабосвязанных органических донорно-акцепторных комплексов могут наблюдаться полосы поглощения, относящиеся к электронному переходу с переносом заряда от донора к акцептору через пространство (межмолекулярный перенос заряда ). Такие комплексы часто называют комплексами с переносом заряда. Длинноволновые полосы поглощения таких комплексов имеют сравнительно низкую интенсивность и могут находиться в ближней УФ, видимой и ближней ИК области спектра.
В металлорганической химии различают полосы поглощения, соответствующие переносу заряда от лиганда к металлу (ПЗЛМ ) и от металла к лиганду (ПЗМЛ ).







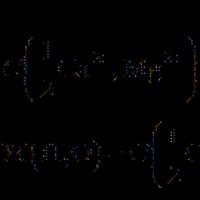 Методика определения ионов кальция и магния в природных водах
Методика определения ионов кальция и магния в природных водах Станьте фокусником с волшебной шляпой!
Станьте фокусником с волшебной шляпой! Кристаллическое строение металлов
Кристаллическое строение металлов Чеченская война: причины и результаты
Чеченская война: причины и результаты Корабль «Виктории» Адмирала Нельсона - это полная подделка Виктория парусник модель журнал
Корабль «Виктории» Адмирала Нельсона - это полная подделка Виктория парусник модель журнал Почему озера не промерзают зимой до дна Почему глубокие водоемы не промерзают до дна
Почему озера не промерзают зимой до дна Почему глубокие водоемы не промерзают до дна Цесаревич и великий князь георгий михайлович
Цесаревич и великий князь георгий михайлович